【0001】
【発明の属する技術分野】
本発明は、機械的強度及び耐湿性に優れる立体造形用組成物、及び立体造形物に関する。
【0002】
【従来の技術】
近年、立体造形物の製造方法として、光学的立体造形用組成物からなる薄膜を形成する工程と、該薄膜に対して光エネルギーを照射し硬化させる工程とを複数回繰り返すことにより、硬化した薄膜を複数積層させ、所望の形状の立体造形物を製造する光学的立体造形法が提案されている(例えば、特許文献1〜4参照)。
【0003】
かかる光学的立体造形法によれば、製造する立体造形物の形状が複雑であっても、簡易にかつ比較的短時間で、所望の立体造形物を製造することができる。光学的立体造形法は、射出成型用金型の試作を行うことなく、3次元CADのデータから直接所望形状のプラスチック部品を試作することが可能であるため、家電機器、自動車等の設計ツールとして普及がすすんだが、最近では設計ツールとして形状確認をするのみならず、得られる光学的立体造形物にて性能テストを実施することが多くなってきている。そのため、光学的立体造形物には、実部品(特にエンジニアリングプラスチック)としての性能も求められつつある。
【0004】
このような光学的立体造形用組成物は、ウレタン(メタ)アクリレート、エポキシ(メタ)アクリレート、ポリエステル(メタ)アクリレート等のオリゴマー類を主成分とする。従って、そのままでは粘度が極めて高く、光学的立体造形用組成物として扱うことは困難である(例えば特許文献5〜7参照)。
そのため一般には、このようなオリゴマー類と、ラジカル重合性不飽和結合を有する低粘度の反応性希釈剤を混合することにより、その取り扱い性を高めている。
しかしながら、その反応性希釈剤は、組成物の硬化速度を低下させる傾向にあり、またそれを用いて得た立体造形物は、実部品としての使用に耐え得る機械的強度や耐湿性等の耐久性のいずれかが劣る傾向にあり、それら全てを満足させることができなかった。
そこで、希釈性能及び硬化性能良好で、かつ機械的強度と耐湿性のバランスに優れる立体造形物を得ることが可能な希釈剤が求められている。
【0005】
【特許文献1】特開昭56−144478号公報
【特許文献2】特開昭60−247515号公報
【特許文献3】特開平3−15520号公報
【特許文献4】特開平3−41126号公報等
【特許文献5】特開平6−199962号公報
【特許文献6】特開平9−316111号公報
【特許文献7】特開2001−310918号公報
【0006】
【発明が解決しようとする課題】
本発明の目的は、粘度が低く、硬化性に優れ、実部品としての使用に耐え得る機械的強度と耐湿性とのバランスに優れた立体造形物を得ることが可能な立体造形用組成物を提供することにある。
【0007】
【課題を解決するための手段】
本発明は、
下記一般式(I)で表される(メタ)アクリル酸エステルを含有する立体造形用組成物、
【0008】
【化2】
(式中、R1は水素原子又はメチル基、R2及びR4は炭素数2〜10のアルキレン基、R3は水素原子、アルキル基、(メタ)アクリロイルオキシアルキル基、シクロアルキル基又は芳香環を有する炭化水素基でありその構造中にエーテル及び/又はエステル結合を含んでいてもよい有機基を示す)
及びそれを硬化して得られる立体造形物である。
【0009】
なお、本発明において「(メタ)アクリル酸」は「アクリル酸又はメタクリル酸」を、「(メタ)アクリロイル基」は「アクリロイル基又はメタクリロイル基」を、「(メタ)アクリレート」は「アクリレート又はメタクリレート」をそれぞれ意味する。
【0010】
【発明の実施の形態】
本発明の立体造形用組成物は、下記一般式(I)で表される(メタ)アクリル酸エステルを含有することを特徴とする。この下記一般式(I)で表される(メタ)アクリル酸エステルは、低粘度でしかも硬化性にも優れることから、非常に取り扱い性にも優れる。また、この下記一般式(I)で表される(メタ)アクリル酸エステルは、得られる立体造形物に、機械的強度(引張強度、引張伸度、引張弾性率)や耐湿性を付与する成分である。
【0011】
【化3】
(式中、R1は水素原子又はメチル基、R2及びR4は炭素数2〜10のアルキレン基、R3は水素原子、アルキル基、(メタ)アクリロイルオキシアルキル基、シクロアルキル基又は芳香環を有する炭化水素基でありその構造中にエーテル及び/又はエステル結合を含んでいてもよい有機基を示す)
【0012】
一般式(I)において、R1は水素原子又はメチル基を表す。特に硬化速度の観点から、水素原子であることが好ましい。R2及びR4は炭素数2〜10のアルキレン基を表す。R2及びR4の炭素数は2以上であることにより、得られる化合物の硬化収縮率が低くなる。
また、炭素数は10以下であることにより、化合物の硬化性が良好となる。R3は水素原子、アルキル基、あるいはシクロアルキル基又は芳香環を有する炭化水素基でありその構造中にエーテル及び/又はエステル結合を含んでいてもよい有機基を示す。
得られる化合物の粘度が低いことから、R3は炭素数10以下の基が好ましく、その中で有機基がより好ましい。
【0013】
一般式(I)で表される(メタ)アクリル酸エステルの具体例としては、例えば、N−メチル−N−2−(メタ)アクリロイルオキシエチル−3−(メタ)アクリロイルオキシプロパナミド、N−メチル−N−2−(メタ)アクリロイルオキシエチル−4−(メタ)アクリロイルオキシブタナミド、N−メチル−N−2−(メタ)アクリロイルオキシエチル−5−(メタ)アクリロイルオキシペンタナミド、N−メチル−N−2−(メタ)アクリロイルオキシエチル−6−(メタ)アクリロイルオキシヘキサナミド、N−エチル−N−2−(メタ)アクリロイルオキシエチル−3−(メタ)アクリロイルオキシプロパナミド、N−エチル−N−2−(メタ)アクリロイルオキシエチル−4−(メタ)アクリロイルオキシブタナミド、N−エチル−N−2−(メタ)アクリロイルオキシエチル−5−(メタ)アクリロイルオキシペンタナミド、N−エチル−N−2−(メタ)アクリロイルオキシエチル−6−(メタ)アクリロイルオキシヘキサナミド、N−2−(メタ)アクリロイルオキシエチル−3−(メタ)アクリロイルオキシプロパナミド、N−2−(メタ)アクリロイルオキシエチル−4−(メタ)アクリロイルオキシブタナミド、N−2−(メタ)アクリロイルオキシエチル−5−(メタ)アクリロイルオキシペンタナミド、N−2−(メタ)アクリロイルオキシエチル−6−(メタ)アクリロイルオキシヘキサナミド、N−メチル−N−2−(メタ)アクリロイルオキシプロピル−3−(メタ)アクリロイルオキシプロパナミド、N−メチル−N−2−(メタ)アクリロイルオキシプロピル−4−(メタ)アクリロイルオキシブタナミド、N−メチル−N−2−(メタ)アクリロイルオキシプロピル−5−(メタ)アクリロイルオキシペンタナミド、N−メチル−N−2−(メタ)アクリロイルオキシプロピル−6−(メタ)アクリロイルオキシヘキサナミド、N−メチル−N−4−(メタ)アクリロイルオキシブチル−3−(メタ)アクリロイルオキシプロパナミド、N−メチル−N−4−(メタ)アクリロイルオキシブチル−4−(メタ)アクリロイルオキシブタナミド、N−メチル−N−4−(メタ)アクリロイルオキシブチル−5−(メタ)アクリロイルオキシペンタナミド、N−メチル−N−4−(メタ)アクリロイルオキシブチル−6−(メタ)アクリロイルオキシヘキサナミド、N,N−ビス(2−アクリロイルオキシエチル)−4−アクリロイルオキシブタナミド、N,N−ビス(3−アクリロイルオキシプロピル)−4−アクリロイルオキシブタナミド、N,N−ビス(4−アクリロイルオキシブチル)−4−アクリロイルオキシブタナミド等が挙げられる。
これらは1種を単独で、または2種以上を併用して用いても良い。
【0014】
一般式(I)で表される(メタ)アクリル酸エステルの製造方法は、特に限定されない。例えば、まず環状ヒドロキシカルボン酸エステルと第一級または第二級アミノ基を含むアミノアルコール化合物とを反応させてアミド基含有アルコールを合成し、このアミド基含有アルコールを前駆体として、一般式(I)で表される(メタ)アクリル酸エステルを得ることができる。
【0015】
環状ヒドロキシカルボン酸エステルの具体例としては、γ−ブチロラクトン、γ−バレロラクトン、δ−バレロラクトン、ε−カプロラクトン等が挙げられる。これらは1種を単独で、または2種以上を併用して用いることができる。
【0016】
第一級または第二級アミノ基を含むアミノアルコール化合物の具体例としては、エタノールアミン、ジエタノールアミン、N−メチルエタノールアミン、N−エチルエタノールアミン、N−フェニルエタノールアミン、2−アミノ−1−ブタノール、2−アミノ−2−エチル−1,3−プロパンジオール、6−アミノ−1−ヘキサノール等が挙げられる。これらは1種を単独で、または2種以上を併用して用いることができる。その中でも、エタノールアミン、ジエタノールアミン、N−メチルエタノールアミンが、得られる化合物の粘度が低くなる点から、特に好ましい。
【0017】
環状ヒドロキシカルボン酸エステルと、第一級または第二級アミノ基を含むアミノアルコール化合物の反応は、例えば、当量比となるように両者を混合し、90〜100℃で6時間以上加熱することにより行うことができる。
【0018】
以上のようにして合成したアミド基含有アルコールを前駆体として、一般式(I)で表される(メタ)アクリル酸エステルを製造する方法としては、例えば、触媒の存在下、(メタ)アクリル酸と脱水エステル化する方法、あるいは、エステル交換触媒の存在下、(メタ)アクリル酸エステル類とのエステル交換反応を行う方法等がある。
【0019】
本発明においては、重合性成分として一般式(I)で表される(メタ)アクリル酸エステルのみ使用し、これに開始剤等を添加して組成物を調製することもできる。ただし、一般式(I)で表される(メタ)アクリル酸エステルは、反応性希釈剤としても非常に良好に機能するものである。したがって、一般式(I)で表される(メタ)アクリル酸エステルだけでなく、それ以外の重合性成分、例えば、以下に詳述するようなオリゴマー、他の反応性モノマー等を適宜混合して、本発明の組成物とすることも好ましい。
本発明の組成物において、一般式(I)で表される(メタ)アクリル酸エステルの含有量は、硬化性や希釈効果の観点から、組成物100質量%中に5〜60質量%の範囲であることが好ましく、10〜40質量%の範囲であることがより好ましい。
【0020】
本発明の組成物には、一般式(I)で表される(メタ)アクリル酸エステルと共に、目的に応じて他のオリゴマーを併用することもできる。
【0021】
他のオリゴマーとしては、ウレタン(メタ)アクリレート系オリゴマー、エポキシ(メタ)アクリレート系オリゴマー、ポリエステル(メタ)アクリレート系オリゴマー等、本発明の組成物の要求性能を考慮して、適宜選択すればよい。
【0022】
例えばウレタン(メタ)アクリレート系オリゴマーの具体例としては、例えば、1,5−ジイソシアナトペンタン、1,6−ジイソシアナトヘキサン、1,4−ジイソシアナトペンタン、1,6−ジイソシアナト−3,5,5−トリメチルヘキサン、1,6−ジイソシアナト−3,3,5−トリメチルヘキサン、1,12−ジイソシアナトドデカン、1,8−ジイソシアナト−4−イソシアナトメチルオクタン、1,3,6−トリイソシアナトヘキサン、1,6,11−トリイソシアナトウンデカン、イソホロンジイソシアネート、トリレンジイソシアネート、キシリレンジイソシアネート、水添キシリレンジイソシアネート、テトラメチルキシリレンジイソシアネート、ジフェニルメタンジイソシアネート、水添ジフェニルメタンジイソシアネート、ナフタレンジイソシアネート、ノルボルナンジイソシアネート、デカリンジイソシアネート、リジンジイソシアネート、リジントリイソシアネート等のイソシアネート化合物と、ポリエチレングリコール、ポリプロピレングリコール、ポリテトラメチレングリコール、ビスフェノールAのエチレンオキサイド付加物、ビスフェノールAのプロピレンオキサイド付加物、ポリエステルポリオール、ポリカーボネートジオール等のポリオール化合物と、2−ヒドロキシエチル(メタ)アクリレート、2−ヒドロキシプロピル(メタ)アクリレート、4−ヒドロキシブチル(メタ)アクリレート、ポリエチレングリコールモノ(メタ)アクリレート、ポリプロピレングリコールモノ(メタ)アクリレート等の水酸基を持つ(メタ)アクリレート化合物とを反応させたウレタン(メタ)アクリレート系オリゴマー;
【0023】
1,5−ジイソシアナトペンタン、1,6−ジイソシアナトヘキサン(HDI)、1,4−ジイソシアナトペンタン、1,6−ジイソシアナト−3,5,5−トリメチルヘキサン、1,6−ジイソシアナト−3,3,5−トリメチルヘキサン、1,12−ジイソシアナトドデカン、1,8−ジイソシアナト−4−イソシアナトメチルオクタン、1,3,6−トリイソシアナトヘキサン、1,6,11−トリイソシアナトウンデカンヘキサ、イソホロンジイソシアネート、トリレンジイソシアネート、キシリレンジイソシアネート、水添キシリレンジイソシアネート、テトラメチルキシリレンジイソシアネート、ジフェニルメタンジイソシアネート、水添ジフェニルメタンジイソシアネート、ナフタレンジイソシアネート、ノルボルナンジイソシアネート、デカリンジイソシアネート、リジンジイソシアネート、リジントリイソシアネート等のイソシアネート化合物の単量体又は多量体に、2−ヒドロキシエチル(メタ)アクリレート、2−ヒドロキシプロピル(メタ)アクリレート、4―ヒドロキシブチル(メタ)アクリレートやそれらのカプロラクトン付加体等の水酸基を有する(メタ)アクリレートを付加したウレタン(メタ)アクリレート系オリゴマー等が挙げられる。
【0024】
エポキシ(メタ)アクリレート系オリゴマーの具体例としては、例えば、フェノールノボラック型エポキシ、クレゾールノボラック型エポキシ、ビスフェノールA型エポキシ、ビスフェノールF型エポキシ等のグリシジルエーテル化合物に(メタ)アクリル酸又はその誘導体を反応させたエポキシポリ(メタ)アクリレート系オリゴマー等が挙げられる。
【0025】
ポリエステル(メタ)アクリレート系オリゴマーの具体例としては、例えば、フタル酸、テトラヒドロフタル酸、ヘキサヒドロフタル酸、アジピン酸等の多塩基酸、エチレングリコール、プロピレングリコール、ネオペンチルグリコール、1,6−ヘキサンジオール、ポリエチレングリコール、ポリプロピレングリコール、ポリテトラメチレングリコール、ビスフェノールA等の多価アルコール、及び(メタ)アクリル酸又はその誘導体との反応で得られるポリエステル(メタ)アクリレート系オリゴマー等が挙げられる。
これらは1種を単独で、または2種以上を併用して用いても良い。
【0026】
本発明の組成物において、これら他のオリゴマーの含有量は、取り扱い性に優れる粘度に調整でき、かつ硬化性にも優れることから、本発明の組成物100質量%中に10〜60質量%が好ましく、15〜50質量%がより好ましい。
【0027】
また本発明の組成物には、一般式(I)で表される(メタ)アクリル酸エステルと共に、目的に応じて他のモノマーを併用することもできる。
【0028】
他のモノマーの具体例としては、例えば、スチレン、α−メチルスチレン、α−クロロスチレン、ビニルトルエン、ジビニルベンゼン等の芳香族ビニル系モノマー;N−ビニル−2−ピロリドン、N−ビニルカプロラクタム等のビニルモノマー;フェニルビニルエーテル等のビニルエーテル;ジアリルフタレート、アリルグリシジルエーテル等のアリル系化合物;アクリロイルモルホリン等のアクリルアミド系化合物;(メタ)アクリル酸テトラヒドロフルフリル、(メタ)アクリル酸ベンジル、(メタ)アクリル酸シクロヘキシル、(メタ)アクリル酸フェノキシエチル、(メタ)アクリル酸トリシクロデカニル、(メタ)アクリル酸ジシクロペンテニル、(メタ)アクリル酸イソボルニル、(メタ)アクリル酸フェニル等のモノ(メタ)アクリレート系化合物;
【0029】
ジシクロペンタンジオールジ(メタ)アクリレート、ジシクロペンタンジメタノールジ(メタ)アクリレート、シクロヘキサンジメタノールジ(メタ)アクリレート、シクロヘキサンジメタノールのエチレンオキサイド付加物のジ(メタ)アクリレート、ジシクロペンタンジオールのカプロラクトン付加物のジ(メタ)アクリル酸エステル、ビスフェノールAのカプロラクトン付加物のジ(メタ)アクリル酸エステル、ビスフェノールFのカプロラクトン付加物のジ(メタ)アクリル酸エステル、ネオペンチルグリコール変性トリメチロールプロパンジ(メタ)アクリル酸エステル、ビスフェノールAエチレンオキサイド付加物のジ(メタ)アクリル酸エステル、ビスフェノールAプロピレンオキサイド付加物のジ(メタ)アクリル酸エステル、ビスフェノールFエチレンオキサイド付加物のジ(メタ)アクリル酸エステル、ビスフェノールFプロピレンオキサイド付加物のジ(メタ)アクリル酸エステル等のジ(メタ)アクリレート、N,N’−ビス(アクリロキシエチル)−N”−ヒドロキシエチルイソシアヌレート等のジ(メタ)アクリレート系化合物;
【0030】
N,N’,N”−トリス((メタ)アクリロキシポリ(エトキシ)エチル)イソシアヌレート等のポリ(メタ)アクリレート、N,N’,N”−トリス(アクリロキシエチル)イソシアヌレート等のトリ(メタ)アクリレート系化合物;
ビスフェノールAグリシジルエーテル、ビスフェノールFグリシジルエーテル、フェノールノボラック型エポキシ、クレゾールノボラック型エポキシ、トリグリシジルトリス(2−ヒドロキシエチル)イソシアヌレート等の分子内に複数のエポキシ基を有するポリエポキシ化合物と(メタ)アクリル酸との付加反応により得られるエポキシポリ(メタ)アクリレート系化合物;
フタル酸、テトラヒドロフタル酸、ヘキサヒドロフタル酸等のポリカルボン酸とエチレングリコール、ポリエチレングリコール(繰り返し単位数:2〜14)、プロピレングリコール、ポリプロピレングリコール(繰り返し単位数:2〜14)、ブチレングリコール、ポリブチレングリコール(繰り返し単位数:2〜14)、ビスフェノールAエチレンオキサイド付加物、トリメチロールプロパン、ペンタエリスリトール等のポリオール(OH官能基数:2〜4)から選ばれる2種以上と(メタ)アクリル酸とを縮合反応させて得られるポリエステルポリ(メタ)アクリレート系化合物等が挙げられる。
これらは1種を単独で、または2種以上を併用して用いても良い。
【0031】
本発明の組成物において、これら他のモノマーの含有量は、得られる光造形物の強伸度特性が向上する傾向にあることから、本発明の組成物100質量%中に、5〜85質量%が好ましく、20〜50質量%がより好ましい。
【0032】
また、本発明の組成物は、エポキシ化合物、オキセタン化合物、ビニルエーテル化合物等の光カチオン重合性モノマーを配合することにより、ハイブリット系組成物にすることも可能である。本発明の組成物をハイブリッド系とすれば、さらに粘度が低減し、取り扱い性が向上する傾向にあり好ましい。
【0033】
光カチオン重合性モノマーの具体例としては、例えば脂環式エポキシ:3,4−エポキシシクロヘキシルメチル−3,4−エポキシシクロヘキサンカルボキシレート、ビス−(3,4−エポキシシクロヘキシル)アジペート、変性脂環式エポキシ、脂肪族系エポキシ:1,2−エポキシシクロデカン、多官能脂環式エポキシ、ビスフェノールA型エポキシ、ビスフェノールF型エポキシ、水添ビスフェノールA型エポキシ、フェノール−ノボラック型エポキシ、オキセタン化合物:3−エチル−3−ヒドロキシメチルオキセタン、1,4−ビス[(3−エチル−3−オキセタニルメトキシ)メチル]ベンゼン、ビニルエーテル化合物:2−エチルヘキシルビニルエーテル、ブタンジオール−1,4−ジビニルエーテル、シクロヘキサンジメタノールモノビニルエーテル、ジエチレングリコールモノ又はジビニルエーテル、ジプロピレングリコールジビニルエーテル、ドデシルビニルエーテル、エチルビニルエーテル、ヘキサンジオールジビニルエーテル、ヒドロキシエチルビニルエーテル、プロピレンカーボネートプロペニルエーテル、プロピルビニルエーテル、トリエチレングリコールジビニルエーテル、ビニル−4−ヒドロキシブチルエーテル、ビニルシクロヘキシルエーテル、ビニルプロピオネート等が挙げられる。
これらは1種を単独で、または2種以上を併用して用いても良い。
【0034】
本発明においてこれらの光カチオン重合性モノマーの含有量は、得られる組成物の粘度が低くかつ硬化性も良好となることから、本発明の組成物100質量%中に5〜70質量%が好ましく、10〜40質量%がより好ましい。
【0035】
本発明の組成物には、硬化速度を向上させる目的で、熱重合開始剤や光重合開始剤等の各種重合開始剤を添加して用いてもよい。
【0036】
熱重合開始剤の具体例としては、例えばメチルエチルケトンパーオキサイド、ベンゾイルパーオキサイド、ジクミルパーオキサイド、t−ブチルハイドロパーオキサイド、クメンハイドロパーオキサイド、t−ブチルパーオキシオクトエート、t−ブチルパーオキシベンゾエート、ラウロイルパーオキサイド等の有機過酸化物やアゾビスイソブチロニトリル等のアゾ系化合物、上記過酸化物にN,N−ジメチルアニリン、N,N−ジメチル−p−トルイジン等のアミン類を組み合わせたレドックス重合開始剤が挙げられる。また必要に応じてナフテン酸コバルト、ナフテン酸マンガン、オクチル酸ニッケル等の金属石鹸類も使用可能である。
【0037】
光重合開始剤の具体例としては、例えば、ベンゾフェノン、4,4−ビス(ジエチルアミノ)ベンゾフェノン、2,4,6−トリメチルベンゾフェノン、メチルオルソベンゾイルベンゾエート、4−フェニルベンゾフェノン、t−ブチルアントラキノン、2−エチルアントラキノンや、2,4−ジエチルチオキサントン、イソプロピルチオキサントン、2,4−ジクロロチオキサントン等のチオキサントン類;ジエトキシアセトフェノン、2−ヒドロキシ−2−メチル−1−フェニルプロパン−1−オン、ベンジルジメチルケタール、1−ヒドロキシシクロヘキシル−フェニルケトン、2−メチル−2−モルホリノ(4−チオメチルフェニル)プロパン−1−オン、2−ベンジル−2−ジメチルアミノ−1−(4−モルホリノフェニル)−ブタノン等のアセトフェノン類;ベンゾインメチルエーテル、ベンゾインエチルエーテル、ベンゾインイソプロピルエーテル、ベンゾインイソブチルエーテル等のベンゾインエーテル類;2,4,6−トリメチルベンゾイルジフェニルホスフィンオキサイド、ビス(2,6−ジメトキシベンゾイル)−2,4,4−トリメチルペンチルホスフィンオキサイド、ビス(2,4,6−トリメチルベンゾイル)−フェニルホスフィンオキサイド等のアシルホスフィンオキサイド類、メチルベンゾイルホルメート、1,7−ビスアクリジニルヘプタン、9−フェニルアクリジン等が挙げられる。
これら重合開始剤は1種を単独で、または2種以上を併用して用いてもよい。
【0038】
本発明の組成物において、重合開始剤の添加量は特に限定されないが、組成物中の固形分100質量部に対して0.01〜15質量部であることが好ましく、硬化速度が向上し効率よく硬化させることができることから0.1〜10質量部であることがより好ましい。
【0039】
さらに本発明の組成物には、本発明の趣旨を逸脱しない範囲内において、離型剤、滑剤、可塑剤、酸化防止剤、帯電防止剤、光安定剤、紫外線吸収剤、難燃剤、難燃助剤、重合禁止剤、充填剤、顔料、染料、シランカップリング剤、レベリング剤、消泡剤、蛍光剤、連鎖移動剤等の、各種添加剤を用途に応じて適宜添加できる。
【0040】
特に、一定の膜厚毎に硬化させて積層して立体造形物を得る場合には、光エネルギー源が紫外光であるとき、所望する膜厚以上に紫外光が到達することを防ぐために、本発明の組成物中に紫外線吸収剤を添加することが好ましい。その添加量は、組成物中の固形分100質量部に対し、0.005〜1質量部の範囲であることが好ましい。
【0041】
さらに、本発明の組成物には、得られる立体造形物の性能を損なわない範囲で、必要に応じて有機溶剤や水を添加することもできる。
本発明の組成物を用いれば、公知の光学的立体造形法により、所望の形状の立体造形物を得ることができる。
その中でも、本発明の組成物は、組成物からなる薄膜を形成する工程と、該薄膜に対して光エネルギーを選択的に照射し硬化させる工程とを複数回繰り返すことにより、硬化薄膜を複数積層させ、所望の形状の立体造形物を製造する光学的立体造形法用として好適に用いられる。
【0042】
本発明の組成物は、熱及び/又は光エネルギーを照射することにより硬化させることができる。その中でも、光エネルギーを用いて硬化させる場合には、短時間で硬化し、精密で複雑な構造の物品を得ることができることから好ましい。
なお、ここでいう光エネルギーとは、可視光線、紫外線、赤外線等の活性エネルギー線を意味する。それらの光の種類としては、レーザー光、あるいはレンズやミラー等を用いて得られる収束光、又は非収束光のいずれの場合でもよく、またパルス発振光等の不連続光、又は連続光のいずれの場合でもよい。
【0043】
例えば、本発明の組成物を用いて立体造形物を得る場合、立体造形の方法は特に限定されないが、その中でも、実用可能な精密で複雑な物品を形成できることから、光学的立体造形法が好ましい。
その光学的立体造形法は、予め組成物を充填させた槽内に、物品の形状に応じて適宜光エネルギーを選択的に照射して硬化させ、それを積層することにより、物品を得る方法である。
本発明の組成物に光エネルギーを選択的に照射する方法としては、特に制限されるものではなく、種々の方法を用いることが出来る。
例えばレーザー光、あるいはレンズやミラー等を用いて得られる収束光を走査させながら組成物に照射する手段、あるいは所定のパターンの光透過部を有するマスクを用い、このマスクを介して非収束光を照射する手段等を用いることができる。
その中でも、微細な形状の立体造形物や、高精度で高寸法安定性が要求される立体造形物を得る場合には、光エネルギー源としてレーザー光を用い、これを走査させながら組成物に照射する手段が好ましく、レーザー光がパルス発振光であることがより好ましい。
【0044】
次に本発明の立体造形物について以下説明する。
本発明の立体造形物は、前記した本発明の組成物を重合硬化させることにより得られる硬化物であり、寸法安定性に優れることから精度よく効率よく製造できるものである。
ここでいう硬化物とは、光学的立体造形法により製造された硬化物そのものだけではなく、その後さらに光照射や加熱によるポストキュア等を行い、その機械的特性や形状安定性等を向上させた硬化物も含まれる。
【0045】
またその構造は、単層構造であっても複層構造であってもよく、用いる光学的立体造形法の種類により異なることから、特に限定されるものではない。
【0046】
本発明の立体造形物の具体的な使用例としては、例えば、設計の途中で外観デザインを検証するためのモデル、部品の機能性を確認するためのモデル、実部品として機械製品等に組み込みその性能を確認するためのモデル、型、金型を制作するためのベースモデル、試作金型用の直接型等の作製、等の試作品や実用可能な物品等が挙げられる。
より具体的な用途としては、例えば精密部品、電気・電子部品、家具、建築構造物、自動車用部品、各種容器類、鋳物、金型、母型等のベースモデルや加工用モデル等の製作等が挙げられる。
【0047】
また、本発明の立体造形物の引張強度、引張伸度、引張弾性率、といった機械的強度と耐湿性を兼ね備えたものであり、さらに優れた熱変形温度を有するものである。
その中でも、本発明の立体造形物は、その他例えば家電製品の嵌合部分の設計用部品や、複雑な構造である物品の繰り返し疲労試験等、引張強度、引張伸度、引張弾性率といった機械的強度の評価用試作品として極めて有用である。
【0048】
【実施例】
以下、実施例及び比較例により本願発明を具体的に示す。以下の記載において、「部」は質量部を意味する。
なお、本実施例についての評価項目及び評価方法は以下記載の通りである。
【0049】
[評価方法]
・粘度
得られた組成物について、25℃における粘度をE型粘度計で測定する。その測定値を表1に示す。
【0050】
・機械的強度(引張強度、引張伸度、引張弾性率)
得られた立体造形物について、JIS K 7113に準拠して引張特性(最大点応力、破断点伸度、及びヤング率)を測定し、得られた値を表1に示す。またその値について下記基準に基づき評価する。
<引張強度>
○:最大点応力が30MPa以上
×:最大点応力が30MPa未満
<引張伸度>
○:破断点伸度が5%以上
×:破断点伸度が5%未満
<引張弾性率>
○:ヤング率が1000MPa以上
×:ヤング率が1000MPa未満
【0051】
・熱変形温度
得られた立体造形物について、JIS K7207のA法に準拠して熱変形温度を測定し、得られた値を表1に示す。
【0052】
・耐湿性
得られた立体造形物について、上皿電子天秤((株)エー・アンド・デイ製、商品名:FA−200)を用いて初期の重量(W0)を測定する。
次いで、得られた立体造形物を高温高湿機((株)カトー製、商品名:シルバリーエンペラーTERRA SSE−43TR−A)を用い、40℃で湿度90%の雰囲気下で所定の日数放置した後、初期と同様にして試験後の立体造形物の重量(W1)を測定する。
得られた立体造形物の初期の重量と試験後の重量の値を用い、下記式(1)から重量変化率を算出し、得られた値を吸湿率として表1に示す。またその値について下記基準に基づき評価する。
<吸湿率>
○:7日後の吸湿率が2%以下
×:7日後の吸湿率が2%超
【0053】
【式1】
【0054】
〈合成例1〉
(1)アミド基含有アルコールの合成
N−メチルエタノールアミンを1モル、γ−ブチロラクトンを1モルの比率で混合し、90℃で12時間加熱攪拌することにより、N−メチル−N−2−ヒドロキシエチル−4−ヒドロキシブタナミドを得た。
(2)アクリレートの合成
N−メチル−N−2−ヒドロキシエチル−4−ヒドロキシブタナミドを1モルに対し、メチルアクリレートを10モル、n−ジオクチルスズオキサイドを0.01モルの比率で混合し、還流下に9時間加熱攪拌しながら副生メタノールを留出した。次いでメチルアクリレートを減圧留去することにより、N−メチル−N−2−アクリロイルオキシエチル−4−アクリロイルオキシブタナミド(以下、MAEABと略記)を得た。
【0055】
〈合成例2〉
(1)アミド基含有アルコールの合成
N−メチルエタノールアミンを1モル、ε−カプロラクトンを1モルの比率で混合し、90℃で12時間加熱攪拌することにより、N−メチル−N−2−ヒドロキシエチル−4−ヒドロキシヘキサナミドを得た。
(2)アクリレートの合成
N−メチル−N−2−ヒドロキシエチル−4−ヒドロキシヘキサナミドを1モルに対し、メチルアクリレートを10モル、n−ジオクチルスズオキサイドを0.01モルの比率で混合し、還流下に9時間加熱攪拌しながら副生メタノールを留出させた。次いでメチルアクリレートを減圧留去することにより、N−メチル−N−2−アクリロイルオキシエチル−6−アクリロイルオキシヘキサナミドを得た。
【0056】
〈合成例3〉
(1)アミド基含有アルコールの合成
ジエタノールアミンを1モル、γ−ブチロラクトンを1モルの比率で混合し、90℃で12時間加熱攪拌することにより、N,N−ビス(2−ヒドロキシエチル)−4−ヒドロキシブタナミドを得た。
(2)アクリレートの合成
N,N−ビス(2−ヒドロキシエチル)−4−ヒドロキシブタナミドを1モルに対し、メチルアクリレートを10モル、n−ジオクチルスズオキサイドを0.01モルの重量比率で混合し、還流下に9時間加熱攪拌しながら副生メタノールを留出させた。次いでメチルアクリレートを減圧留去することにより、N,N−ビス(2−アクリロイルオキシエチル)−4−アクリロイルオキシブタナミドを得た。
【0057】
〈実施例1:光学的立体造形用組成物の調製、及び立体造形物の製造〉
合成例1で得たMAEAB30部、オリゴマーとしてウレタンアクリレート(三菱レイヨン(株)製、商品名:ダイヤビームUK−6091)40部、モノマーとしてカプロラクトン変性ヒドロキシピバリン酸エステルネオペンチルグリコール(日本化薬(株)製、商品名:カヤラッドHX−220)20部と東亜合成(株)製アロニックスM−315を10部、重合開始剤として1−ヒドロキシシクロヘキシルフェニルケトン3部、その他成分として、2−(3,5−ジ−t−ブチル−2−ヒドロキシフェニル)ベンゾトリアゾール0.05部を混合し組成物を得た。
得られた組成物を用い、超高速光造形システム(CMET株式会社製、製品名:「SOLIFORM250」)を使用して、LD光(出力100mW、波長365nm)を表面に対して垂直に照射し、スライスピッチ(積層厚み)を0.2mm、1層あたりの平均造形時間を2分として光学的立体造形を行い、JIS7113に準ずるダンベル試験片形状の硬化物を得た。
ここで得られた硬化物をイソプロピルアルコールで洗浄し、それに付着する未硬化の組成物を除去した。その後、それに3kWの紫外線をそれに10分間照射してポストキュアし、立体造形物を得た。
得られた立体造形物について、評価した評価結果は、表1に示す。
【0058】
〈実施例2、3、及び比較例1〜3〉
表1に示す組成及び組成比とする以外は実施例1と同様にして組成物を調製し、それを用いて実施例1と同様の方法で立体造形物を得た。
得られた立体造形物について、評価した評価結果は、表1に示す。
【0059】
【表1】
【0060】
なお、表中、各成分の配合量の単位は「質量部」である。
【0061】
また、表中の略号は下記の通りである。
MAEAB:N−メチル−N−2−アクリロイルオキシエチル−4−アクリロイルオキシブタナミド
MAEAH:N−メチル−N−2−アクリロイルオキシエチル−6−アクリロイルオキシヘキサナミド
BAEAB:N,N−ビス(2−アクリロイルオキシエチル)−4−アクリロイルオキシブタナミド
UK6091:ウレタンアクリレート(三菱レイヨン(株)製、商品名:ダイヤビームUK−6091)
UK6105:ウレタンアクリレート(三菱レイヨン(株)製、商品名:ダイヤビームUK−6105)
M−7100:ポリエステルアクリレート(東亜合成(株)製、商品名:アロニックスM−7100)
HX−220:カプロラクトン変性ヒドロキシピバリン酸エステルネオペンチルグリコール(日本化薬(株)製、商品名:カヤラッドHX−220)
M−315:トリス(アクリロキシエチル)イソシアヌレート(東亜合成(株)製、商品名:アロニックスM−315)
ACMO:アクリロイルモルホリン
*1:1−ヒドロキシシクロヘキシルフェニルケトン
*2:2−(3,5−ジ−t−ブチル−2−ヒドロキシフェニル)ベンゾトリアゾール
【0062】
比較例の考察:
比較例1〜3は、本発明に用いる前記一般式(I)で表される化合物を含まない組成物の例である。いずれの場合にも、低粘度の組成物を得ることができたが、得られた立体造形物の7日後の吸湿率が2%を超えるものであり、低粘度で、かつ得られる立体造形物の機械的強度(引張強度、引張伸度、及び引張弾性率)や耐湿性とを兼ね備える組成物ではなかった。
【0063】
【発明の効果】
以上説明したように、本発明の組成物は、低粘度でありながら硬化性に優れ、しかも実部品としての使用に耐え得る機械的強度(引張強度、引張伸度、及び引張弾性率)と耐湿性とを兼ね備えた立体造形物を得ることができる。
このように優れた性能を有する本発明の組成物は、例えば型の製作用モデル、母型、機械的物性等の試験や評価のための物品、又は設計検討時の試作用物品等の各種用途の他、実部品としても使用可能な立体造形物を形成できる材料として、非常に有用である。[0001]
TECHNICAL FIELD OF THE INVENTION
The present invention relates to a three-dimensional structure composition having excellent mechanical strength and moisture resistance, and a three-dimensional structure.
[0002]
[Prior art]
In recent years, as a method of manufacturing a three-dimensional molded article, a step of forming a thin film made of an optical three-dimensional molding composition and a step of irradiating the thin film with light energy and curing the thin film are repeated a plurality of times to obtain a cured thin film. Are stacked to produce a three-dimensional object having a desired shape (for example, see Patent Documents 1 to 4).
[0003]
According to such an optical three-dimensional molding method, even if the shape of the three-dimensional molded object to be produced is complicated, a desired three-dimensional molded object can be produced simply and in a relatively short time. The optical three-dimensional molding method enables a prototype of plastic parts of a desired shape to be directly produced from three-dimensional CAD data without trial production of a mold for injection molding. Although the use has spread, recently, not only the shape is confirmed as a design tool, but also a performance test is often performed on the obtained optical three-dimensional structure. For this reason, the performance as an actual part (particularly an engineering plastic) is being demanded of an optical three-dimensional structure.
[0004]
Such a composition for optical three-dimensional modeling mainly includes oligomers such as urethane (meth) acrylate, epoxy (meth) acrylate, and polyester (meth) acrylate. Therefore, the viscosity is extremely high as it is, and it is difficult to handle it as a composition for optical three-dimensional modeling (for example, see Patent Documents 5 to 7).
Therefore, in general, such oligomers are mixed with a low-viscosity reactive diluent having a radically polymerizable unsaturated bond to improve the handleability.
However, the reactive diluent tends to reduce the curing speed of the composition, and the three-dimensional molded article obtained using the reactive diluent has mechanical strength and moisture resistance that can withstand use as a real part. Any of the sexes tended to be inferior, and all of them could not be satisfied.
Therefore, a diluent capable of obtaining a three-dimensional structure having good dilution performance and curing performance and excellent balance between mechanical strength and moisture resistance has been demanded.
[0005]
[Patent Document 1] JP-A-56-144478
[Patent Document 2] JP-A-60-247515
[Patent Document 3] JP-A-3-15520
[Patent Document 4] JP-A-3-41126 and the like
[Patent Document 5] JP-A-6-199962
[Patent Document 6] JP-A-9-316111
[Patent Document 7] JP-A-2001-310918
[0006]
[Problems to be solved by the invention]
An object of the present invention is to provide a composition for three-dimensional modeling capable of obtaining a three-dimensional molded article having a low viscosity, excellent curability, and an excellent balance between mechanical strength and moisture resistance that can withstand use as a real part. To provide.
[0007]
[Means for Solving the Problems]
The present invention
A stereolithographic composition containing a (meth) acrylate represented by the following general formula (I),
[0008]
Embedded image
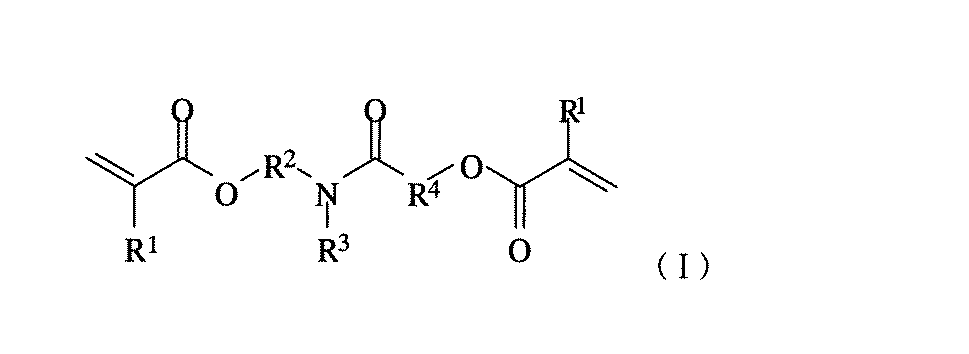
And a three-dimensional structure obtained by curing the same.
[0009]
In the present invention, “(meth) acrylic acid” means “acrylic acid or methacrylic acid”, “(meth) acryloyl group” means “acryloyl group or methacryloyl group”, and “(meth) acrylate” means “acrylate or methacrylate”. ] Respectively.
[0010]
BEST MODE FOR CARRYING OUT THE INVENTION
The three-dimensional structure forming composition of the present invention is characterized by containing a (meth) acrylate represented by the following general formula (I). The (meth) acrylic acid ester represented by the following general formula (I) has a low viscosity and is excellent in curability, so that it is very excellent in handleability. The (meth) acrylate represented by the following general formula (I) is a component that imparts mechanical strength (tensile strength, tensile elongation, tensile modulus) and moisture resistance to the obtained three-dimensional molded article. It is.
[0011]
Embedded image
(Where R 1 Is a hydrogen atom or a methyl group, R 2 And R 4 Is an alkylene group having 2 to 10 carbon atoms, R 3 Is a hydrogen atom, an alkyl group, a (meth) acryloyloxyalkyl group, a cycloalkyl group or a hydrocarbon group having an aromatic ring, and represents an organic group which may have an ether and / or ester bond in its structure.
[0012]
In the general formula (I), R 1 Represents a hydrogen atom or a methyl group. Particularly, from the viewpoint of the curing rate, a hydrogen atom is preferable. R 2 And R 4 Represents an alkylene group having 2 to 10 carbon atoms. R 2 And R 4 Has a carbon number of 2 or more, the curing shrinkage of the obtained compound is reduced.
When the carbon number is 10 or less, the curability of the compound is improved. R 3 Represents a hydrogen atom, an alkyl group, a cycloalkyl group or a hydrocarbon group having an aromatic ring, and an organic group which may have an ether and / or ester bond in its structure.
Due to the low viscosity of the resulting compound, R 3 Is preferably a group having 10 or less carbon atoms, and among them, an organic group is more preferable.
[0013]
Specific examples of the (meth) acrylate represented by the general formula (I) include, for example, N-methyl-N-2- (meth) acryloyloxyethyl-3- (meth) acryloyloxypropanamide, N -Methyl-N-2- (meth) acryloyloxyethyl-4- (meth) acryloyloxybutanamide, N-methyl-N-2- (meth) acryloyloxyethyl-5- (meth) acryloyloxypentanamide, N-methyl-N-2- (meth) acryloyloxyethyl-6- (meth) acryloyloxyhexanamide, N-ethyl-N-2- (meth) acryloyloxyethyl-3- (meth) acryloyloxypropana Amide, N-ethyl-N-2- (meth) acryloyloxyethyl-4- (meth) acryloyloxybutanamide, N-ethyl -N-2- (meth) acryloyloxyethyl-5- (meth) acryloyloxypentanamide, N-ethyl-N-2- (meth) acryloyloxyethyl-6- (meth) acryloyloxyhexanamide, N -2- (meth) acryloyloxyethyl-3- (meth) acryloyloxypropanamide, N-2- (meth) acryloyloxyethyl-4- (meth) acryloyloxybutanamide, N-2- (meth) acryloyl Oxyethyl-5- (meth) acryloyloxypentanamide, N-2- (meth) acryloyloxyethyl-6- (meth) acryloyloxyhexanamide, N-methyl-N-2- (meth) acryloyloxypropyl -3- (meth) acryloyloxypropanamide, N-methyl-N-2- (meth) acrylo Oxypropyl-4- (meth) acryloyloxybutanamide, N-methyl-N-2- (meth) acryloyloxypropyl-5- (meth) acryloyloxypentanamide, N-methyl-N-2- (meth ) Acryloyloxypropyl-6- (meth) acryloyloxyhexanamide, N-methyl-N-4- (meth) acryloyloxybutyl-3- (meth) acryloyloxypropanamide, N-methyl-N-4- (Meth) acryloyloxybutyl-4- (meth) acryloyloxybutanamide, N-methyl-N-4- (meth) acryloyloxybutyl-5- (meth) acryloyloxypentanamide, N-methyl-N-4 -(Meth) acryloyloxybutyl-6- (meth) acryloyloxyhexanamide, N, N-bis (2 -Acryloyloxyethyl) -4-acryloyloxybutanamide, N, N-bis (3-acryloyloxypropyl) -4-acryloyloxybutanamide, N, N-bis (4-acryloyloxybutyl) -4-acryloyloxy Butanamide and the like.
These may be used alone or in combination of two or more.
[0014]
The method for producing the (meth) acrylate represented by the general formula (I) is not particularly limited. For example, first, a cyclic hydroxycarboxylic acid ester is reacted with an amino alcohol compound containing a primary or secondary amino group to synthesize an amide group-containing alcohol, and the amide group-containing alcohol is used as a precursor in the general formula (I) )) Can be obtained.
[0015]
Specific examples of the cyclic hydroxycarboxylic acid ester include γ-butyrolactone, γ-valerolactone, δ-valerolactone, ε-caprolactone, and the like. These can be used alone or in combination of two or more.
[0016]
Specific examples of the amino alcohol compound containing a primary or secondary amino group include ethanolamine, diethanolamine, N-methylethanolamine, N-ethylethanolamine, N-phenylethanolamine, 2-amino-1-butanol. , 2-amino-2-ethyl-1,3-propanediol, 6-amino-1-hexanol and the like. These can be used alone or in combination of two or more. Among them, ethanolamine, diethanolamine, and N-methylethanolamine are particularly preferable because the viscosity of the obtained compound is reduced.
[0017]
The reaction between the cyclic hydroxycarboxylic acid ester and the amino alcohol compound containing a primary or secondary amino group can be performed, for example, by mixing the two at an equivalent ratio and heating the mixture at 90 to 100 ° C. for 6 hours or more. It can be carried out.
[0018]
As a method for producing the (meth) acrylic ester represented by the general formula (I) using the amide group-containing alcohol synthesized as described above as a precursor, for example, (meth) acrylic acid is used in the presence of a catalyst. And a method of performing a transesterification reaction with (meth) acrylic esters in the presence of a transesterification catalyst.
[0019]
In the present invention, a composition can also be prepared by using only a (meth) acrylate represented by the general formula (I) as a polymerizable component and adding an initiator and the like thereto. However, the (meth) acrylate represented by the general formula (I) functions very well also as a reactive diluent. Therefore, not only the (meth) acrylate represented by the general formula (I) but also other polymerizable components such as oligomers and other reactive monomers described in detail below are appropriately mixed. The composition of the present invention is also preferable.
In the composition of the present invention, the content of the (meth) acrylate represented by the general formula (I) is in the range of 5 to 60% by mass in 100% by mass of the composition from the viewpoint of curability and dilution effect. And more preferably in the range of 10 to 40% by mass.
[0020]
In the composition of the present invention, other oligomers can be used in combination with the (meth) acrylate represented by the general formula (I) according to the purpose.
[0021]
Other oligomers such as urethane (meth) acrylate-based oligomers, epoxy (meth) acrylate-based oligomers, and polyester (meth) acrylate-based oligomers may be appropriately selected in consideration of the required performance of the composition of the present invention.
[0022]
For example, specific examples of urethane (meth) acrylate oligomers include, for example, 1,5-diisocyanatopentane, 1,6-diisocyanatohexane, 1,4-diisocyanatopentane, 1,6-diisocyanato-3 , 5,5-Trimethylhexane, 1,6-diisocyanato-3,3,5-trimethylhexane, 1,12-diisocyanatododecane, 1,8-diisocyanato-4-isocyanatomethyloctane, 1,3,6 -Triisocyanatohexane, 1,6,11-triisocyanatoundecane, isophorone diisocyanate, tolylene diisocyanate, xylylene diisocyanate, hydrogenated xylylene diisocyanate, tetramethyl xylylene diisocyanate, diphenylmethane diisocyanate, hydrogenated diphenylmethane diisocyanate Isocyanate compounds such as catenate, naphthalene diisocyanate, norbornane diisocyanate, decalin diisocyanate, lysine diisocyanate, and lysine triisocyanate; polyethylene glycol, polypropylene glycol, polytetramethylene glycol, ethylene oxide adduct of bisphenol A, propylene oxide adduct of bisphenol A, Polyol compounds such as polyester polyol and polycarbonate diol, 2-hydroxyethyl (meth) acrylate, 2-hydroxypropyl (meth) acrylate, 4-hydroxybutyl (meth) acrylate, polyethylene glycol mono (meth) acrylate, and polypropylene glycol mono ( (Meth) acrylic having hydroxyl group such as (meth) acrylate Urethane obtained by reacting a over preparative Compound (meth) acrylate oligomer;
[0023]
1,5-diisocyanatopentane, 1,6-diisocyanatohexane (HDI), 1,4-diisocyanatopentane, 1,6-diisocyanato-3,5,5-trimethylhexane, 1,6-diisocyanato -3,3,5-trimethylhexane, 1,12-diisocyanatododecane, 1,8-diisocyanato-4-isocyanatomethyloctane, 1,3,6-triisocyanatohexane, 1,6,11-tri Isocyanatoundecane hexa, isophorone diisocyanate, tolylene diisocyanate, xylylene diisocyanate, hydrogenated xylylene diisocyanate, tetramethyl xylylene diisocyanate, diphenylmethane diisocyanate, hydrogenated diphenylmethane diisocyanate, naphthalene diisocyanate, norbornane diiso 2-hydroxyethyl (meth) acrylate, 2-hydroxypropyl (meth) acrylate, 4-hydroxybutyl (meth) acrylate And urethane (meth) acrylate oligomers to which a (meth) acrylate having a hydroxyl group such as a caprolactone adduct thereof has been added.
[0024]
Specific examples of the epoxy (meth) acrylate oligomer include, for example, reacting (meth) acrylic acid or a derivative thereof with a glycidyl ether compound such as phenol novolak type epoxy, cresol novolak type epoxy, bisphenol A type epoxy, bisphenol F type epoxy, Epoxy poly (meth) acrylate oligomers and the like.
[0025]
Specific examples of the polyester (meth) acrylate oligomer include, for example, polybasic acids such as phthalic acid, tetrahydrophthalic acid, hexahydrophthalic acid, adipic acid, ethylene glycol, propylene glycol, neopentyl glycol, and 1,6-hexane. Examples thereof include polyhydric alcohols such as diol, polyethylene glycol, polypropylene glycol, polytetramethylene glycol, and bisphenol A, and polyester (meth) acrylate oligomers obtained by reaction with (meth) acrylic acid or a derivative thereof.
These may be used alone or in combination of two or more.
[0026]
In the composition of the present invention, the content of these other oligomers can be adjusted to a viscosity excellent in handleability and excellent in curability, so that 10 to 60% by mass in 100% by mass of the composition of the present invention. Preferably, it is 15 to 50% by mass.
[0027]
In the composition of the present invention, other monomers can be used in combination with the (meth) acrylate represented by the general formula (I) according to the purpose.
[0028]
Specific examples of other monomers include, for example, aromatic vinyl monomers such as styrene, α-methylstyrene, α-chlorostyrene, vinyltoluene, and divinylbenzene; N-vinyl-2-pyrrolidone, N-vinylcaprolactam, and the like. Vinyl monomers; vinyl ethers such as phenyl vinyl ether; allyl compounds such as diallyl phthalate and allyl glycidyl ether; acrylamide compounds such as acryloyl morpholine; tetrahydrofurfuryl (meth) acrylate, benzyl (meth) acrylate, and (meth) acrylic acid Mono (meth) amines such as cyclohexyl, phenoxyethyl (meth) acrylate, tricyclodecanyl (meth) acrylate, dicyclopentenyl (meth) acrylate, isobornyl (meth) acrylate, and phenyl (meth) acrylate Acrylate compounds;
[0029]
Dicyclopentanediol di (meth) acrylate, dicyclopentanedimethanol di (meth) acrylate, cyclohexanedimethanol di (meth) acrylate, di (meth) acrylate of ethylene oxide adduct of cyclohexanedimethanol, dicyclopentanediol Caprolactone adduct di (meth) acrylate, bisphenol A caprolactone adduct di (meth) acrylate, bisphenol F caprolactone adduct di (meth) acrylate, neopentylglycol-modified trimethylolpropane (Meth) acrylic acid ester, di (meth) acrylic acid ester of bisphenol A ethylene oxide adduct, di (meth) acrylic acid ester of bisphenol A propylene oxide adduct Di (meth) acrylates such as di (meth) acrylate of bisphenol F ethylene oxide adduct and di (meth) acrylate of bisphenol F propylene oxide adduct, N, N'-bis (acryloxyethyl)- A di (meth) acrylate compound such as N "-hydroxyethyl isocyanurate;
[0030]
Poly (meth) acrylates such as N, N ′, N ″ -tris ((meth) acryloxypoly (ethoxy) ethyl) isocyanurate and tris such as N, N ′, N ″ -tris (acryloxyethyl) isocyanurate (Meth) acrylate compounds;
Bisphenol A glycidyl ether, bisphenol F glycidyl ether, phenol novolak type epoxy, cresol novolak type epoxy, triglycidyl tris (2-hydroxyethyl) isocyanurate, and other polyepoxy compounds having a plurality of epoxy groups in the molecule and (meth) acrylic An epoxy poly (meth) acrylate compound obtained by an addition reaction with an acid;
Polycarboxylic acids such as phthalic acid, tetrahydrophthalic acid and hexahydrophthalic acid, and ethylene glycol, polyethylene glycol (number of repeating units: 2 to 14), propylene glycol, polypropylene glycol (number of repeating units: 2 to 14), butylene glycol, (Meth) acrylic acid and two or more kinds selected from polyols (OH functional groups: 2 to 4) such as polybutylene glycol (number of repeating units: 2 to 14), bisphenol A ethylene oxide adduct, trimethylolpropane, and pentaerythritol And polyester poly (meth) acrylate compounds obtained by a condensation reaction of
These may be used alone or in combination of two or more.
[0031]
In the composition of the present invention, the content of these other monomers is 5 to 85% by mass in 100% by mass of the composition of the present invention since the strength and elongation characteristics of the obtained optically shaped article tend to be improved. % Is preferable, and 20 to 50% by mass is more preferable.
[0032]
The composition of the present invention can also be made into a hybrid composition by blending a cationic photopolymerizable monomer such as an epoxy compound, an oxetane compound, or a vinyl ether compound. It is preferable that the composition of the present invention is a hybrid system, because the viscosity is further reduced and the handleability is improved.
[0033]
Specific examples of the photocationically polymerizable monomer include, for example, alicyclic epoxy: 3,4-epoxycyclohexylmethyl-3,4-epoxycyclohexanecarboxylate, bis- (3,4-epoxycyclohexyl) adipate, modified alicyclic Epoxy, aliphatic epoxy: 1,2-epoxycyclodecane, polyfunctional alicyclic epoxy, bisphenol A epoxy, bisphenol F epoxy, hydrogenated bisphenol A epoxy, phenol-novolak epoxy, oxetane compound: 3- Ethyl-3-hydroxymethyloxetane, 1,4-bis [(3-ethyl-3-oxetanylmethoxy) methyl] benzene, vinyl ether compound: 2-ethylhexyl vinyl ether, butanediol-1,4-divinyl ether, cyclohexanedimeta Monovinyl ether, diethylene glycol mono or divinyl ether, dipropylene glycol divinyl ether, dodecyl vinyl ether, ethyl vinyl ether, hexanediol divinyl ether, hydroxyethyl vinyl ether, propylene carbonate propenyl ether, propyl vinyl ether, triethylene glycol divinyl ether, vinyl-4-hydroxy Butyl ether, vinylcyclohexyl ether, vinyl propionate and the like.
These may be used alone or in combination of two or more.
[0034]
In the present invention, the content of these photocationic polymerizable monomers is preferably 5 to 70% by mass in 100% by mass of the composition of the present invention, since the resulting composition has a low viscosity and good curability. , 10 to 40% by mass.
[0035]
To the composition of the present invention, various polymerization initiators such as a thermal polymerization initiator and a photopolymerization initiator may be added for the purpose of improving the curing rate.
[0036]
Specific examples of the thermal polymerization initiator include, for example, methyl ethyl ketone peroxide, benzoyl peroxide, dicumyl peroxide, t-butyl hydroperoxide, cumene hydroperoxide, t-butyl peroxy octoate, t-butyl peroxy benzoate. And organic peroxides such as lauroyl peroxide and azo compounds such as azobisisobutyronitrile, and the above peroxides combined with amines such as N, N-dimethylaniline and N, N-dimethyl-p-toluidine. Redox polymerization initiator. If necessary, metal soaps such as cobalt naphthenate, manganese naphthenate and nickel octylate can also be used.
[0037]
Specific examples of the photopolymerization initiator include, for example, benzophenone, 4,4-bis (diethylamino) benzophenone, 2,4,6-trimethylbenzophenone, methylorthobenzoylbenzoate, 4-phenylbenzophenone, t-butylanthraquinone, Ethylanthraquinone, thioxanthones such as 2,4-diethylthioxanthone, isopropylthioxanthone and 2,4-dichlorothioxanthone; diethoxyacetophenone, 2-hydroxy-2-methyl-1-phenylpropan-1-one, benzyldimethylketal, 1-hydroxycyclohexyl-phenyl ketone, 2-methyl-2-morpholino (4-thiomethylphenyl) propan-1-one, 2-benzyl-2-dimethylamino-1- (4-morpholinophenyl) -bu Benzoin ethers such as benzoin methyl ether, benzoin ethyl ether, benzoin isopropyl ether and benzoin isobutyl ether; 2,4,6-trimethylbenzoyldiphenylphosphine oxide, bis (2,6-dimethoxybenzoyl) -2 Acylphosphine oxides such as 4,4,4-trimethylpentylphosphine oxide, bis (2,4,6-trimethylbenzoyl) -phenylphosphine oxide, methylbenzoyl formate, 1,7-bisacridinyl heptane, 9-phenyl Acridine and the like.
These polymerization initiators may be used alone or in combination of two or more.
[0038]
In the composition of the present invention, the amount of the polymerization initiator to be added is not particularly limited, but is preferably 0.01 to 15 parts by mass with respect to 100 parts by mass of the solid content in the composition, and the curing rate is improved and the efficiency is improved. It is more preferable that the amount is 0.1 to 10 parts by mass because it can be cured well.
[0039]
Further, the composition of the present invention may include a releasing agent, a lubricant, a plasticizer, an antioxidant, an antistatic agent, a light stabilizer, an ultraviolet absorber, a flame retardant, and a flame retardant within a range not departing from the gist of the present invention. Various additives such as an auxiliary agent, a polymerization inhibitor, a filler, a pigment, a dye, a silane coupling agent, a leveling agent, a defoaming agent, a fluorescent agent, and a chain transfer agent can be appropriately added depending on the application.
[0040]
In particular, when a three-dimensional object is obtained by curing and curing at a constant film thickness to obtain a three-dimensional molded object, when the light energy source is ultraviolet light, it is necessary to prevent the ultraviolet light from reaching the desired film thickness or more. It is preferred to add an ultraviolet absorber to the composition of the invention. The addition amount is preferably in the range of 0.005 to 1 part by mass with respect to 100 parts by mass of the solid content in the composition.
[0041]
Further, an organic solvent or water can be added to the composition of the present invention, if necessary, as long as the performance of the obtained three-dimensional structure is not impaired.
When the composition of the present invention is used, a three-dimensional structure having a desired shape can be obtained by a known optical three-dimensional structure method.
Among them, the composition of the present invention is formed by laminating a plurality of cured thin films by repeating a process of forming a thin film composed of the composition and a process of selectively irradiating light energy to the thin film and curing the thin film a plurality of times. Then, it is suitably used for an optical three-dimensional molding method for producing a three-dimensional molded article having a desired shape.
[0042]
The composition of the present invention can be cured by irradiating heat and / or light energy. Among them, it is preferable to use light energy for curing, since it can be cured in a short time and an article having a precise and complicated structure can be obtained.
Here, the light energy means an active energy ray such as visible light, ultraviolet light, or infrared light. The type of the light may be any of laser light, convergent light obtained using a lens or a mirror, or non-convergent light, or discontinuous light such as pulsed light, or continuous light. May be the case.
[0043]
For example, when obtaining a three-dimensional molded article using the composition of the present invention, the method of three-dimensional modeling is not particularly limited, and among them, an optical three-dimensional modeling method is preferable because a practical and precise article can be formed. .
The optical three-dimensional molding method is a method of obtaining an article by selectively irradiating light energy appropriately according to the shape of the article in a tank previously filled with the composition, curing the light energy, and laminating it. is there.
The method for selectively irradiating the composition of the present invention with light energy is not particularly limited, and various methods can be used.
For example, a means for irradiating the composition while scanning convergent light obtained using a laser beam or a lens or a mirror, or a mask having a light transmitting portion of a predetermined pattern, and non-convergent light through this mask is used. Irradiation means and the like can be used.
Among them, when obtaining a three-dimensional object with a fine shape or a three-dimensional object requiring high precision and high dimensional stability, use a laser beam as an optical energy source and irradiate the composition while scanning it. Preferably, the laser beam is pulsed light.
[0044]
Next, the three-dimensional structure of the present invention will be described below.
The three-dimensional structure of the present invention is a cured product obtained by polymerizing and curing the above-described composition of the present invention, and can be accurately and efficiently produced because of its excellent dimensional stability.
The cured product referred to here is not only the cured product itself manufactured by the optical three-dimensional molding method, but also post-curing by light irradiation or heating and the like to improve its mechanical properties and shape stability. Cured products are also included.
[0045]
The structure may be a single-layer structure or a multi-layer structure, and is not particularly limited since it differs depending on the type of the optical three-dimensional molding method used.
[0046]
Specific examples of the use of the three-dimensional structure of the present invention include, for example, a model for verifying an external design during design, a model for confirming the functionality of a part, and a real part incorporated into a mechanical product or the like. Prototypes such as a model for confirming performance, a base model for producing a mold, a mold, and a direct mold for a prototype mold, and practically usable articles, and the like.
More specific applications include, for example, the production of precision parts, electrical and electronic parts, furniture, building structures, automotive parts, various containers, castings, molds, molds, base models such as molds, processing models, and the like. Is mentioned.
[0047]
Further, the three-dimensional structure of the present invention has both mechanical strength such as tensile strength, tensile elongation, and tensile elasticity, and moisture resistance, and further has an excellent heat deformation temperature.
Among them, the three-dimensional molded article of the present invention includes other mechanical parts such as tensile strength, tensile elongation, tensile modulus, and the like, such as a part for designing a fitting portion of a home appliance and a repeated fatigue test of an article having a complicated structure. It is extremely useful as a prototype for evaluating strength.
[0048]
【Example】
Hereinafter, the present invention will be specifically described with reference to Examples and Comparative Examples. In the following description, “parts” means parts by mass.
The evaluation items and the evaluation method for this example are as described below.
[0049]
[Evaluation method]
·viscosity
About the obtained composition, the viscosity in 25 degreeC is measured with an E-type viscometer. Table 1 shows the measured values.
[0050]
・ Mechanical strength (tensile strength, tensile elongation, tensile modulus)
The tensile properties (maximum point stress, elongation at break, and Young's modulus) of the obtained three-dimensional structure were measured in accordance with JIS K 7113, and the obtained values are shown in Table 1. The value is evaluated based on the following criteria.
<Tensile strength>
:: Maximum point stress is 30 MPa or more
X: The maximum point stress is less than 30 MPa.
<Tensile elongation>
:: elongation at break is 5% or more
×: Elongation at break less than 5%
<Tensile modulus>
:: Young's modulus is 1000 MPa or more
×: Young's modulus is less than 1000 MPa
[0051]
・ Heat deformation temperature
For the obtained three-dimensional structure, the heat distortion temperature was measured in accordance with the method A of JIS K7207, and the obtained values are shown in Table 1.
[0052]
・ Moisture resistance
The initial weight (W) of the obtained three-dimensional molded object was measured using a precision electronic balance (trade name: FA-200, manufactured by A & D Corporation). 0 ) Is measured.
Next, the obtained three-dimensional structure was left for a predetermined number of days at 40 ° C. in an atmosphere of 90% humidity using a high-temperature and high-humidity machine (trade name: Silvery Emperor TERRA SSE-43TR-A, manufactured by Kato Corporation). After that, the weight of the three-dimensional structure after the test (W 1 ) Is measured.
Using the values of the initial weight and the weight after the test of the obtained three-dimensional structure, a weight change rate was calculated from the following equation (1), and the obtained value is shown in Table 1 as a moisture absorption rate. The value is evaluated based on the following criteria.
<Moisture absorption rate>
:: moisture absorption after 7 days is 2% or less
×: Moisture absorption after 7 days exceeded 2%
[0053]
(Equation 1)
[0054]
<Synthesis Example 1>
(1) Synthesis of amide group-containing alcohol
1 mol of N-methylethanolamine and 1 mol of γ-butyrolactone are mixed and heated and stirred at 90 ° C. for 12 hours to obtain N-methyl-N-2-hydroxyethyl-4-hydroxybutanamide. Was.
(2) Synthesis of acrylate
1 mol of N-methyl-N-2-hydroxyethyl-4-hydroxybutanamide, 10 mol of methyl acrylate and 0.01 mol of n-dioctyltin oxide are mixed at a ratio of 1 mol, and heated under reflux for 9 hours. By-product methanol was distilled off with stirring. Then, methyl acrylate was distilled off under reduced pressure to obtain N-methyl-N-2-acryloyloxyethyl-4-acryloyloxybutanamide (hereinafter abbreviated as MAEAB).
[0055]
<Synthesis Example 2>
(1) Synthesis of amide group-containing alcohol
N-methylethanolamine was mixed at a ratio of 1 mol and ε-caprolactone at a ratio of 1 mol, and the mixture was heated and stirred at 90 ° C. for 12 hours to give N-methyl-N-2-hydroxyethyl-4-hydroxyhexanamide. Obtained.
(2) Synthesis of acrylate
For 1 mol of N-methyl-N-2-hydroxyethyl-4-hydroxyhexanamide, 10 mol of methyl acrylate and 0.01 mol of n-dioctyltin oxide were mixed at a ratio of 1 mol, and the mixture was refluxed for 9 hours. Methanol by-product was distilled off with heating and stirring. Then, methyl acrylate was distilled off under reduced pressure to obtain N-methyl-N-2-acryloyloxyethyl-6-acryloyloxyhexanamide.
[0056]
<Synthesis Example 3>
(1) Synthesis of amide group-containing alcohol
1 mol of diethanolamine and 1 mol of γ-butyrolactone were mixed and heated and stirred at 90 ° C. for 12 hours to obtain N, N-bis (2-hydroxyethyl) -4-hydroxybutanamide.
(2) Synthesis of acrylate
N, N-Bis (2-hydroxyethyl) -4-hydroxybutanamide was mixed with 1 mole of methyl acrylate and 0.01 mole of n-dioctyltin oxide with respect to 1 mole, and the mixture was refluxed with 9 moles. By-product methanol was distilled off while heating and stirring for an hour. Then, methyl acrylate was distilled off under reduced pressure to obtain N, N-bis (2-acryloyloxyethyl) -4-acryloyloxybutanamide.
[0057]
<Example 1: Preparation of composition for optical three-dimensional modeling and production of three-dimensional molded article>
30 parts of MAEAB obtained in Synthesis Example 1, 40 parts of urethane acrylate (trade name: Diabeam UK-6091, manufactured by Mitsubishi Rayon Co., Ltd.) as an oligomer, and caprolactone-modified hydroxypivalate ester neopentyl glycol (Nippon Kayaku Co., Ltd.) as a monomer 20 parts of Kayarad HX-220), 10 parts of Aronix M-315 manufactured by Toagosei Co., Ltd., 3 parts of 1-hydroxycyclohexyl phenyl ketone as a polymerization initiator, and 2- (3,3) as other components. 0.05 part of 5-di-t-butyl-2-hydroxyphenyl) benzotriazole was mixed to obtain a composition.
Using the obtained composition, LD light (output: 100 mW, wavelength: 365 nm) was irradiated perpendicularly to the surface using an ultra-high-speed stereolithography system (manufactured by CMET, product name: “SOLIFORM250”). Optical three-dimensional molding was performed with a slice pitch (layer thickness) of 0.2 mm and an average molding time per layer of 2 minutes to obtain a cured product in the form of a dumbbell specimen according to JIS7113.
The cured product obtained here was washed with isopropyl alcohol to remove the uncured composition adhering thereto. Thereafter, it was post-cured by irradiating it with ultraviolet light of 3 kW for 10 minutes to obtain a three-dimensional structure.
Table 1 shows the results of the evaluation of the obtained three-dimensional structure.
[0058]
<Examples 2, 3 and Comparative Examples 1 to 3>
A composition was prepared in the same manner as in Example 1 except that the composition and composition ratio shown in Table 1 were used, and a three-dimensional structure was obtained using the composition in the same manner as in Example 1.
Table 1 shows the results of the evaluation of the obtained three-dimensional structure.
[0059]
[Table 1]
[0060]
In the table, the unit of the amount of each component is “parts by mass”.
[0061]
Abbreviations in the table are as follows.
MAEAB: N-methyl-N-2-acryloyloxyethyl-4-acryloyloxybutanamide
MAEAH: N-methyl-N-2-acryloyloxyethyl-6-acryloyloxyhexanamide
BAEAB: N, N-bis (2-acryloyloxyethyl) -4-acryloyloxybutanamide
UK6091: urethane acrylate (manufactured by Mitsubishi Rayon Co., Ltd., trade name: Diabeam UK-6091)
UK6105: urethane acrylate (manufactured by Mitsubishi Rayon Co., Ltd., trade name: Diabeam UK-6105)
M-7100: Polyester acrylate (manufactured by Toagosei Co., Ltd., trade name: ARONIX M-7100)
HX-220: caprolactone-modified hydroxypivalic acid ester neopentyl glycol (manufactured by Nippon Kayaku Co., Ltd., trade name: Kayarad HX-220)
M-315: Tris (acryloxyethyl) isocyanurate (manufactured by Toagosei Co., Ltd., trade name: Aronix M-315)
ACMO: Acryloylmorpholine
* 1: 1-hydroxycyclohexyl phenyl ketone
* 2: 2- (3,5-di-t-butyl-2-hydroxyphenyl) benzotriazole
[0062]
Discussion of Comparative Example:
Comparative Examples 1 to 3 are examples of compositions not containing the compound represented by the general formula (I) used in the present invention. In each case, a low-viscosity composition could be obtained, but the moisture absorption after 7 days of the obtained three-dimensional structure was more than 2%, and the low-viscosity and three-dimensional structure obtained were obtained. It was not a composition having both mechanical strength (tensile strength, tensile elongation, and tensile modulus) and moisture resistance.
[0063]
【The invention's effect】
As described above, the composition of the present invention has low viscosity, excellent curability, and mechanical strength (tensile strength, tensile elongation and tensile elasticity) and moisture resistance that can withstand use as an actual part. It is possible to obtain a three-dimensional object having both properties.
The composition of the present invention having such excellent performance can be used for various purposes such as, for example, a mold production model, a master mold, an article for testing and evaluation of mechanical properties and the like, or a prototype article for design study. In addition, it is very useful as a material capable of forming a three-dimensional structure that can be used as an actual part.